Autor: Hellmut Nordwig
Sprecherin und Sprecher: Ilka Teichmüller, Rosario Bona und Birgit Paul
Regie: Stefanie Lazai
Technik: Sonja Rebel
Redaktion: Martin Mair
Die Verantwortung der Ärzte

Wann dient das Verschreiben von Medikamenten nur dem Wohl des Patienten, ab wann füllt es im hohen Maße die Taschen der Ärztinnen und Ärzte? © Getty images / fStop / Malte Müller
Das Geschäft mit Medikamentenstudien
30:19 Minuten

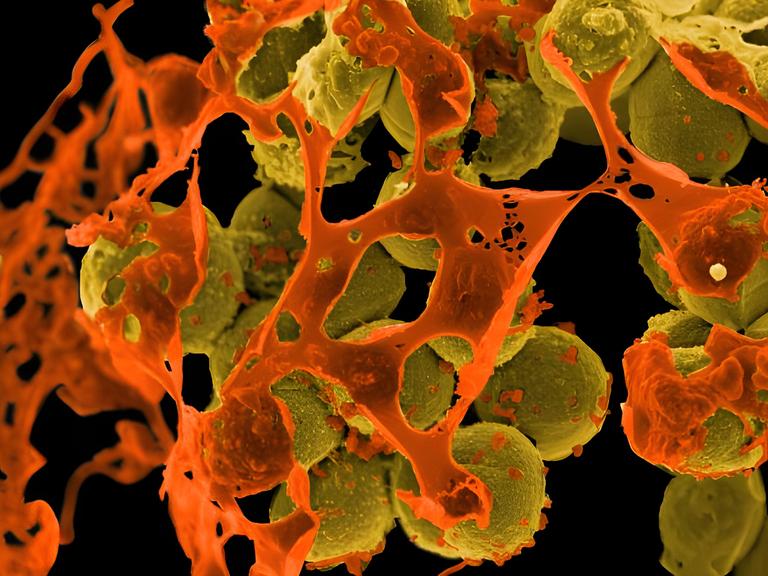
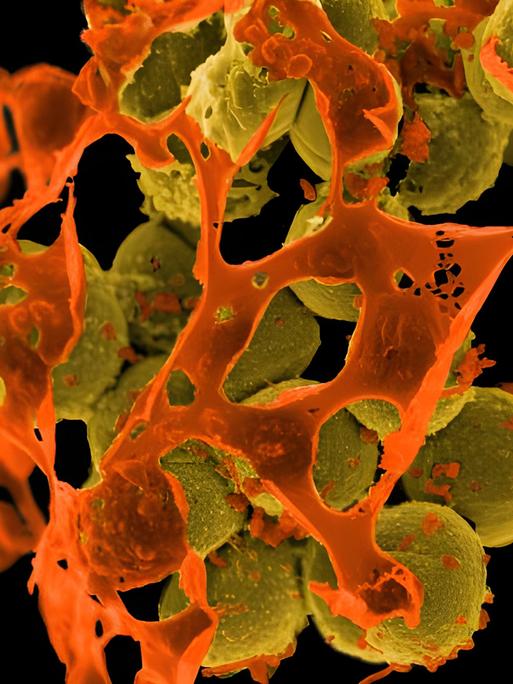
Die Wirkung von Medikamenten im Alltag zu beobachten, ist für die Ärzteschaft ein lohnender Zusatzverdienst. Pharmafirmen zahlen für Studien, deren wissenschaftlicher Nutzen fraglich ist. Die Patienten erfahren wenig darüber.
Das Berufsgericht für Heilberufe in Berlin: Am 18. Mai 2018 verurteilt die Kammer einen niedergelassenen Internisten zu einer Geldstrafe. Er hat von einem Unternehmen Geld angenommen, das im Auftrag einer Pharmafirma arbeitet, und seinen Patienten ein Medikament verschrieben, das genau diese Firma herstellt.
In der Urteilsbegründung heißt es: "Der Beschuldigte nahm von der Firma R. Geldzuwendungen in Höhe von mindestens 60.250 Euro an. Soweit diese Zuwendungen als Vergütung für von dem Beschuldigten dokumentierte Anwendungsbeobachtungen bestimmt gewesen sein sollten, war diese Vergütung im Verhältnis zu den hierfür von ihm erbrachten Leistungen unangemessen hoch. Er hat damit – zu seinen Gunsten – bezogen auf 122 Anwendungsbeobachtungen zumindest 37.454 Euro unangemessen erhalten, wobei der Durchschnittsbetrag bereits überhöht erscheint."
"Beispiel für korruptionsnahe Element"
Das Gericht kann dem Arzt nicht nachweisen, dass er die Zahlung direkt für die Verordnung erhalten hat. Offiziell ist das Geld dafür geflossen, dass der Mediziner im Auftrag des Unternehmens beobachtet hat, wie sich das Präparat im Alltag verhält. Doch die Summe, die er kassierte, war deutlich zu hoch, so das Gericht.
"Anwendungsbeobachtungen sind, jedenfalls, wenn man die früheren Diskussionen zugrunde legt, geradezu ein Anschauungsbeispiel dafür gewesen korruptionsnahe Elemente im Pharmavertrieb aufzuzeigen", sagt Ralf Kölbel. Er ist Professor für Strafrecht und Kriminologie an der Universität München, Schwerpunkt: Wirtschaftskriminalität. "Im Rahmen von Anwendungsbeobachtungen – so die damalige Annahme – lassen sich Zuwendungen an die Ärzte vonseiten der Herstellerunternehmen relativ gut tarnen. Gleichzeitig lässt sich auf diese Weise ein verschreibungsstimulierender Effekt herbeiführen."
Ralf Kölbel formuliert vorsichtig, schließlich ist er Jurist. Er spricht von "damals" – von den Jahren 2007 bis 2010. Um diese Zeit ging es in dem Verfahren vor dem Berliner Berufsgericht für Heilberufe. Damals also hätten einige Pharmafirmen zumindest nahe an der Korruption gehandelt, "indem man Verträge mit den Ärzten abschließt, die dann an so einer Anwendungsbeobachtung teilnehmen, und indem man ihnen für diese Teilnahme ein Honorar zahlt". Das Honorar habe den Aufwand überstiegen, der mit der Teilnahme an so einer Anwendungsbeobachtung verbunden gewesen seien.
Pharmaindustrie zahlt Millionen
Im Klartext: Die Pharmaindustrie soll also Ärztinnen und Ärzten für bloße Alltagsbeobachtungen ihrer Medikamente so viel bezahlt haben, dass Mediziner genau dieses Präparat verschreiben. Für Patientinnen und Patienten bedeutet das: Sie hätten nicht immer die beste Behandlung bekommen, sondern eine, die für den Arzt besonders lukrativ ist.
Ein schwerer Vorwurf, der "damals" in der Tat manchmal zutraf. Das räumt Thorsten Ruppert vom Verband forschender Arzneimittelhersteller ein. Er fügt aber hinzu: Heute sei das anders. "Es gibt die gesetzlichen Regelungen, es gibt die Empfehlung der Bundesoberbehörden, und die gelten für alle. Da kann sich keiner in irgendeiner Form rausziehen." Auf der anderen Seite gebe es eine klare Transparenz über die geleisteten Zahlungen. Die Krankenkassen etwa wüssten Bescheid. "Von daher sehen wir, dass diese alte Kritik – die früher teilweise berechtigt war – nicht mehr zeitgemäß ist."
Doch die sogenannten Anwendungsbeobachtungen gibt es nach wie vor. Das zeigt eine Liste der Kassenärztlichen Bundesvereinigung. Die oberste Interessenvertretung der niedergelassenen Mediziner weist 45 solcher Studien für 2019 aus. Pharmafirmen haben dafür insgesamt rund 7 Millionen Euro an mehr als 2000 Ärzte gezahlt.
Alltagscheck zum Patientenwohl?
Herbert Schreiber ist einer dieser Ärzte, die im Auftrag von Pharmakonzernen Erkenntnisse über deren Medikamente zusammentragen. Der Professor für Neurologie behandelt vor allem Menschen mit Multipler Sklerose und Demenzkrankheiten.
Es ist Freitagnachmittag in seiner Ulmer Praxis, die letzten Patienten sind längst weg. Er blättert in einem Ordner. "Es gibt einen sogenannten Zentrumsordner. Dort sind die ganzen administrativen Dinge abgelegt, also etwa Verträge oder das Studienprotokoll, um objektive Daten zu generieren." Außerdem gebe es meistens noch sogenannte Patientenordner. "Hier haben wir zum Beispiel einen Ordner, in dem fünf Patienten dieser nicht interventionellen Studie enthalten sind. Die enthalten die gesamten Dokumente über die Behandlungszeit."
Herbert Schreiber findet es wichtig, "nicht interventionelle Studien" zu machen, wie die Anwendungsbeobachtungen auch genannt werden. Soll heißen: Der Arzt behandelt seine Patientinnen und Patienten so wie immer. Er ändert also nichts an der Therapie. Aber er dokumentiert sie – ohne Patientennamen – für die Firma, die ihn beauftragt hat. "Da geht es um klinische Daten, um klinische Untersuchungsbefunde. Da wird gefragt nach Vortherapien, nach Zusatzerkrankungen. Dann kommen ganz bestimmte Tests, die bei der ersten Untersuchung anonym erhoben werden. Dann gibt es Folgeuntersuchungen. Nach drei Monaten, nach sechs Monaten und so weiter."
Nicht zuletzt gehört eine schriftliche Einverständniserklärung der Patientin oder des Patienten in den Ordner. Noch ist nichts ausgefüllt. Sonst dürfte Herbert Schreiber ihn nicht zeigen, selbst wenn die Namen der Erkrankten nicht auftauchen. Das Unternehmen hat mit ihm nämlich vereinbart, dass alles geheim bleibt. Das ist üblich bei solchen Beobachtungen und Voraussetzung dafür, dass der Neurologe die Unterlagen überhaupt bekommt.
Im Lauf der Zeit wird er mit den Daten von fünf Erkrankten einen ganzen Ordner für die Firma füllen. Es sei nicht so, dass man einfach ein wenig arbeite, und die dicke Vergütung einschiebe, sagt Schreiber. "Es ist alles ziemlich klar reglementiert. Die Firmen müssen im Zweifelsfall den Wirtschaftsprüfern Rechenschaft ablegen. Die Ethikkommissionen schauen drüber. Es wird an die Behörden gemeldet. Das ist keine Welt, wie man sie von der Börse kennt, von Wirecard oder so, da können Sie sicher sein."

"Das ist keine Welt, wie man sie von der Börse kennt, von Wirecard oder so", sagt der Arzt Herbert Schreiber über das Geschäft mit medizinischen Studien. © Getty Images / iStock / Sasha Brazhnik
Strenge Regeln, die keinen Spielraum mehr für Korruption zulassen sollen. Die Firma kann vorab eine Ethikkommission einschalten, die auch die Honorare für die Ärzte erfährt und prüfen kann, ob sie angemessen sind. Nur: Verpflichtend ist das nicht. Es passiert aber meistens. Immer muss eine Anwendungsbeobachtung jedoch den Krankenkassen und Aufsichtsbehörden gemeldet werden. Entweder dem Bundesinstitut für Arzneimittel und Medizinprodukte oder dem Paul-Ehrlich-Institut. Die veröffentlichen dann, dass sie stattfindet.
Kontrollgremien auf freiwilliger Basis
Im Fall von Herbert Schreiber geht es um ein Medikament gegen Multiple Sklerose. Bevor das Präparat zugelassen wurde, haben Forschende bereits eine Studie in mehreren Phasen mit einigen Tausend Patienten gemacht. Sie war Voraussetzung, dass das Mittel überhaupt auf den Markt kommen konnte. Aber es gebe Grenzen dieser treuen Studien – etwa in der Zusammensetzung der Versuchsteilnehmer.
"Die sind oft jünger als die Populationen in der breiten Medizin", sagt Schreiber. "Die haben weniger Begleiterkrankungen oder auch Begleitmedikationen. Die beeinflussen letztlich ja auch mein Behandlungsergebnis." Erfahrungen aus dem bunten Querschnitt einer Praxis sind es also, die der Internist zusammenträgt. Mit jüngeren und älteren Patienten, mit Menschen, die nicht nur an Multipler Sklerose leiden, sondern zum Beispiel zugleich an Diabetes oder Herzschwäche, und mit Schwangeren. Die werden von den Zulassungsstudien bewusst ausgeschlossen.
Genau diese Alltagserfahrungen sind aus Sicht der Industrie wichtig, sagt Thorsten Ruppert. Anwendungsbeobachtungen hätten eben einen Stellenwert zur Vertiefung von Erkenntnissen über ein Arzneimittel nach seiner Zulassung unter Alltagsbedingungen. "Ich mache immer folgenden Vergleich auf: Wenn man einen Löwen im Zoo beobachtet, kann man sehr viel über Löwen lernen, aber eben auch nicht alles. Denn er wird jeden Tag zum Beispiel pünktlich um 14 Uhr gefüttert. Man kennt die Tiere, mit denen er zusammenlebt. Erst, wenn man einen Löwen in der freien Wildbahn beobachtet, lernt man, wie er jagt, wie er mit Hunger umgeht – also eben den Alltag eines Löwen." Das könne man ganz gut als Analogie nutzen für eine klinische Prüfung unter Anwendungsbeobachtung als Vergleich.
Umstrittener wissenschaftlicher Nutzen
Doch sind die Beobachtungen im Auftrag der Industrie wirklich nötig? Sind sie aus wissenschaftlicher Sicht wertvoll? Jürgen Windeler hat dazu eine klare Meinung, und seine Antworten haben Gewicht. Er leitet in Köln das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen. Seine Aufträge kommen vom Bundesgesundheitsministerium und von einem Gremium, das darüber entscheidet, was die gesetzlichen Krankenkassen zahlen und was nicht.
Nach Meinung von Jürgen Windeler kann man Anwendungsbeobachtungen, "Forschungsschrott nennen, den man nicht braucht". Die Kölner Experten des Instituts verzichten bewusst auf die Daten aus Anwendungsbeobachtungen, wenn sie Medikamente wissenschaftlich bewerten. Denn diese tragen dazu einfach nichts bei, sagt Windeler.
Er erzählt von einem Beispiel: Ärzte haben 1000 Migränepatienten beobachtet. Alle haben ein bestimmtes Medikament bekommen. Es gab aber keinen Vergleich mit einem Placebo – also einem Mittel ohne Wirkstoff – oder mit einer anderen Therapie. Genau das unterscheidet Anwendungsbeobachtungen durch Ärzte von richtigen klinischen Studien.
Das Ergebnis: Das Migränemittel hilft gegen die Schmerzen. "Bloß die entscheidende Frage, die man natürlich hat: Ist das stärker vermindert, als wenn die Patienten einfach spazieren gegangen wären, Entspannungstherapien gemacht hätten, ein anderes Medikament eingenommen hätten? Diese Aussage ist also gar nicht verwertbar, nicht interpretierbar. Das weiß der Autor auch ganz genau, er schreibt nämlich. Jetzt hat man diesen Effekt beobachtet und müsste ihn noch in einer richtigen, ordentlichen, vergleichenden Studie bestätigen." Die Forschenden sind also so schlau wie vorher.
Neues Medikament zum Nachteil des Patienten?
Und was haben die Patientinnen und Patienten von all dem? Sie sollen zumindest keinen Nachteil erleiden. Deshalb ist vorgeschrieben, dass sie das Medikament bereits bekommen, bevor der Arzt anfängt zu dokumentieren, wie es sich bei ihnen auswirkt.
Das soll verhindern, dass sie ein Präparat eigens deswegen erhalten. Im Extremfall sogar statt eines anderen Medikaments, mit dem sie gut zurechtgekommen sind und das ihnen geholfen hat. Das klingt selbstverständlich – ist es aber nicht.
2004 hat die Europäische Arzneimittelbehörde das Insulinpräparat Apidra zugelassen. Im Sommer 2016 begann die Herstellerfirma Sanofi mit einer Anwendungsbeobachtung. 79 Ärzte haben teilgenommen und insgesamt 415 Patienten beobachtet. Sanofi hat ihnen pro Patient bis zu 375 Euro bezahlt. Dabei hat das Unternehmen einen Stundensatz von 75 Euro zugrunde gelegt, der bei Ärzten als üblich gilt.
Das Ergebnis der Daten: Nach einem Jahr konnte die Hälfte der Patienten ihren Zielwert für den Blutzucker erreichen. Auch in diesem Fall gab es keine Vergleichsgruppe. Außerdem haben viele der beobachteten Patienten zusätzlich weitere Diabetes-Medikamente eingenommen. Deshalb ist nicht sicher, ob die Blutzuckersenkung wirklich nur auf Apidra zurückzuführen ist.
Für Wolfgang Dietrich, Internist und Hausarzt in München mit Schwerpunkt Diabetes, ist klar: Das ist kein brauchbares Ergebnis. Es werde nicht einmal deutlich, dass Apidra wenigstens nicht schlechter ist als andere Insuline.
Noch dazu seien hier die Patienten auf das Medikament "umgestellt" worden. "Und man kann sich dann fragen, ob diese Umstellung und Neueinstellung dadurch veranlasst ist, dass der Arzt denkt, dass das im besten Sinn des Patienten ist – oder ob er dabei an sein Honorar für die Anwendungsbeobachtung denkt."
Die Antwort darauf fällt schwer: Denn eine Umstellung auf ein anderes Insulin-Präparat ist manchmal nötig in der Diabetesbehandlung – mit oder ohne Anwendungsbeobachtung. Der Hersteller von Apidra jedenfalls weist die Vermutung zurück, dass Ärzte es nur deswegen verschreiben, weil ihnen Geld für die Beobachtung winke.
Hersteller sehen keine Beeinflussung
In den Unterlagen für die Ärzte hieß es dazu, die Mediziner müssten die Entscheidung für die Umstellung unabhängig von der Studie treffen. Aber länger als zwei Wochen dürfe es nicht her sein, dass die Patienten auf das neue Medikament umgestellt wurden.
Dieter Paar, der medizinische Direktor von Sanofi sagt: "Worüber man nicht diskutieren kann, ist, dass die Patienten vor Einschluss in die Anwendungsbeobachtung die Verordnung erhalten haben müssen und nicht wegen des Einschlusses in die Anwendungsbeobachtung. Ich glaube nicht, dass es so schwierig ist, das voneinander zu trennen, weil man ja auf dem Dokumentationsbogen sieht, wie lange der Patient auf dem Arzneimittel ist."
Man könne also sehr wohl nachvollziehen, dass die Umstellung nicht mit der Anwendungsbeobachtung in Zusammenhang stehe. Sanofi lege großen Wert darauf zu erfahren, wie seine Medikamente im "wahren Leben" wirken, sagt Dieter Paar, und das selbst dann, wenn ein Präparat schon lange auf dem Markt ist.
Die Anwendungsbeobachtung von Apidra zum Beispiel begann erst zwölf Jahre nach der Zulassung. "Manche Ärzte sagen: Eigentlich wissen wir ja schon alles zu dem Arzneimittel. Wir als Hersteller oder unsere externen Studienleiter sagen: Wir wissen noch nicht alles. Wir wissen nicht, in welcher Geschwindigkeit dosiert wird, wie schnell sich der Blutzucker senkt. Solche genauen Untersuchungen wird man in der täglichen Anwendung ohne eine Anwendungsbeobachtung nie so genau dokumentieren."
Dieter Paar glaubt deshalb: Die klinischen Studien zur Zulassung eines neuen Medikamentes allein reichten nicht aus. Ein Wirkstoff wird in einem aufwendigen Verfahren in drei Phasen geprüft, ehe er auf den Markt kommt. Es geht um die Fragen, ob das Mittel wirkt, um Risiken und Nebenwirkungen. Dieses Zulassungsverfahren folgt hohen wissenschaftlichen Standards und schließt verschiedene Patientengruppen ein.
Geben Anwendungsbeobachtung wertvolle Zusatzinformationen über ein Medikament – oder sind sie überflüssig? Darüber gehen die Meinungen auseinander.© imago images / fStop Images / Malte Müller
Doch danach brauche es auch Erkenntnisse aus dem Therapiealltag, findet der medizinische Direktor von Sanofi, und verdeutlicht seine Meinung an einem Beispiel für ein Insulin, das zur Behandlung von Patienten mit Typ-I-Diabetes entwickelt wurde. Der Körper der Erkrankten kann kein Insulin mehr bilden.
"Man hat in den letzten Jahren für diese Patienten die kontinuierliche Glukosemessung mit Pads entwickelt, die unter der Haut, meist am Oberarm, getragen werden. "Wir haben für dieses Insulin aus den Zulassungsstudien, weil es damals diese Methode der Blutzuckermessung noch gar nicht so gab, nicht sehr viele, oder ehrlich gesagt sogar sehr wenige Daten. Da bin ich der Meinung, dass wir auch jetzt in einer einarmigen nicht interventionellen Studie sehr davon profitieren."
"Wichtige Erkenntnisse aus dem Therapiealltag"
Also davon, Patienten ohne Vergleichsgruppe zu beobachten. Die Wissenschaft profitiere zwar auch, wenn es eine Kontrollgruppe gebe. Aber solche Studien sind viel aufwendiger und damit teurer.
Beides habe seine Berechtigung, sagt Dieter Paar. Die Daten von Anwendungsbeobachtungen verschwänden ja auch nicht einfach in der Schublade: "Sie können es heute nicht riskieren, so etwas nicht zu veröffentlichen. Wenn Sie in das Register eingestellt haben, dass Sie die durchführen, und in zwei Jahren sagt jemand: Wo ist eigentlich das Ergebnis – das fängt man nicht ein. Ich glaube, da gibt es keinen Ausweg mehr. Das muss veröffentlicht werden."
Es ist aber die Frage, wie. Im Arzneimittelgesetz ist vorgeschrieben, dass die zuständige Behörde einen Abschlussbericht erhält. Die veröffentlicht den – etwas versteckt – auf ihren Webseiten.
Wissenschaftliche Publikationen in Fachzeitschriften sind aber nicht die Regel. Bei der Anwendungsbeobachtung von Apidra sei sie in Vorbereitung, schreibt Dieter Paar nach unserem Interview auf Anfrage.
Der Münchner Diabetologe Wolfgang Dietrich kontert: Er sei gespannt, ob das wirklich irgendein Fachmedium interessant genug finde. Aus seiner Sicht hat die Beobachtung einen ganz anderen Zweck. Hier gehe es darum, dass der Arzt etwas macht, das er nach seiner Auffassung und der vieler Kollegen, gar nicht machen sollte. "Der Arzt sollte sich nicht dafür bezahlen lassen, dass er dem Patienten ein bestimmtes Arzneimittel verordnet, auch wenn das hinter der Kulisse einer Studie oder einer Beobachtung oder wie auch immer man das nennen will, versteckt wird. Noch dazu verordnet man ja in der Regel auf einem Kassenrezept oder einem Privatrezept, sprich zulasten der gesetzlichen Krankenkasse oder zulasten der Privatkasse oder der Patienten selber."
Anwendungsbeobachtungen sind umstritten. Das dürfte schon das Einzige sein, worauf sich Gegner und Befürworter einigen können. Sie liefern wichtige Erkenntnisse, sagen die einen. Kritiker halten dagegen: Die wissenschaftliche Qualität sei bescheiden, Patienten könnten womöglich nicht das geeignetste Medikament bekommen, und der Arzt verschreibe eher ein Präparat, das er für eine Firma beobachtet, weil er dafür ja Geld erhält.
Doch: Lässt sich das nachweisen? Eine neue Studie hat es versucht. Geleitet hat sie Klaus Lieb, Professor an der Klinik für Psychiatrie der Universität Mainz. Knapp 7000 Ärztinnen und Ärzte haben teilgenommen. Die Forschenden konnten so prüfen: Wie ändert sich das Verordnungsverhalten bei Ärzten und Ärzten, die an einer Anwendungsbeobachtung teilgenommen haben im Vergleich zur Kontrollgruppe, wo das nicht der Fall war.
Anwendungsbeobachtungen kurbeln Umsatz an
Das Ergebnis: Ärzte verschreiben ein Medikament tatsächlich häufiger, wenn sie von der Pharmafirma für eine Anwendungsbeobachtung Geld bekommen, und zwar sogar noch ein Jahr, nachdem die Studie beendet ist.
Der Effekt ist scheinbar klein: Es geht um eine Zunahme von etwa sechs bis acht Prozent. "Man kann natürlich argumentieren, dass acht Prozent Zunahme nicht so relevant ist", sagt Klaus Lieb. "Aber, wenn man sich mal überlegt: Wenn ich irgendwo Produktzuwächse habe von acht Prozent durch eine einfache Maßnahme, finde ich die nicht irrelevant. Wenn man auch bedenkt, dass wir sehr hohe Arzneimittelpreise haben, ist acht Prozent nicht wenig."
Der Hersteller kann mit einer Anwendungsbeobachtung also sein Medikament häufiger verkaufen. Nur: Hat das auch nachweisbar Folgen für die Patientinnen und Patienten? Klaus Lieb verweist darauf, dass dies nicht direkter Gegenstand der Studie war.
Er ist deshalb zurückhaltend mit einer abschließenden Einschätzung: "Wo es verschiedene Optionen gibt, vorrangig aber das Medikament der Anwendungsbeobachtung verordnet wird, kann das für den Patienten schon ein Schaden sein. Es kann aber auch andersrum sein. Es kann sein, dass das Anwendungsbeobachtungsmedikament tatsächlich besser ist und dann auch der Patient davon einen Nutzen hat."
Gefährliche Nebenwirkungen
Es gibt allerdings einen Fall, bei dem schwere Nebenwirkungen eines Medikaments zutage getreten sind – und wo Anwendungsbeobachtungen trotzdem weitergeführt wurden.
Daclizumab ist ein Präparat, das zwei US-Firmen gemeinsam gegen Multiple Sklerose entwickelt haben, 2016 wurde es dafür zugelassen. In diesem Jahr begannen Anwendungsbeobachtungen in Deutschland mit 620 Patienten. 113 Ärzte waren beteiligt. Insgesamt haben die Unternehmen ihnen fast eine halbe Million Euro bezahlt, im Schnitt rund 800 Euro pro Patient.
Das neue Präparat war sehr teuer. Es gab Alternativen. Bereits kurz nach der Zulassung kam es zu einem Todesfall. Ab Mitte 2017 warnte die europäische Zulassungsbehörde EMA vor der weiteren Verwendung. Trotzdem liefen die Anwendungsbeobachtungen weiter. Im Mai 2018 wurde das Präparat von der EMA verboten.
Kann es sein, dass hier ein teures Medikament mithilfe von Anwendungsbeobachtungen in den Markt gedrückt wurde? Und das, obwohl schnell der Verdacht bestand, es ist gefährlich? Zwei Anfragen hat die US-Firma AbbVie, die den ursprünglichen Hersteller übernommen hat, nicht beantwortet. Auch das Unternehmen Biogen schweigt. Es war an der Entwicklung des Präparats ebenfalls beteiligt.
Offiziell bestreitet die Industrie, dass sie mit den Anwendungsbeobachtungen auf höhere Umsätze abzielt. Doch wer in die Fachliteratur schaut, bekommt ein anderes Bild. So hat zum Beispiel Thomas Trilling, Geschäftsführer einer Biotechnologie-Firma, 2015 ein Buch mit dem Titel "Pharmamarketing" herausgegeben.
Studien und den bezahlten Beobachtungen widmet er dort ein eigenes Kapitel. Darin heißt es, es empfehle sich, Ärzte als Teilnehmer für ein neues Präparat zu gewinnen oder die als Meinungsbildner weitere Ärzte beeinflussen könnten.
Dieter Paar, der medizinische Direktor bei Sanofi, hatte im telefonischen Vorgespräch gesagt: Anwendungsbeobachtungen als Marketing, das sei zwar "nicht die Denke" forschender Hersteller. Aber als "Nebenwirkung" könne es doch mal mehr Verschreibungen geben.
Woran liegt es, dass Ärzte ein Medikament häufiger verordnen, wenn sie es für die Industrie beobachten?© Getty Images / fStop / Malte Müller
Im Interview darauf angesprochen, sagt er: "Das habe ich vielleicht in der Tat ansatzweise so gesagt. Ich habe eigentlich etwas anderes gemeint. Wenn die Ergebnisse gut sind, wenn man zum Beispiel sieht: Dieses Insulin sorgt für einen sehr stabilen Blutzuckerspiegel, die Patienten haben weniger Unter- oder Überzuckerung, dann wird selbstverständlich die Folge sein, dass auch das Vertrauen in dieses Insulin in der Ärzteschaft, die die Studie gelesen hat, zunehmen wird."
Woran genau es liegt, dass Ärzte ein Medikament häufiger verordnen, wenn sie es für die Industrie beobachten – das haben Klaus Lieb und seine Kolleginnen in ihrer Studie nicht untersucht. Fest steht: Mediziner lassen sich beeinflussen. Das allein ist für manche Grund genug, sich nicht daran zu beteiligen.
Wie beeinflussbar ist die Ärzteschaft?
Herbert Schreiber zieht für sich einen anderen Schluss. Er sei im Alltag ständig Beeinflussungen ausgesetzt. Es gehe darum, sie auszutarieren und eine möglichst rationale Haltung einzunehmen: "Das ist für den Arzt genauso. Er kann ja auch manchmal zwischen zwei, drei Medikamenten auswählen. Das ist natürlich schwierig. In einem solchen Fall kann es schon einmal vorkommen, dass ein Arzt vielleicht mal ein Präparat nimmt, das er in einer Anwendungsbeobachtung gerade prüft."
Da der wissenschaftliche Nutzen zumindest umstritten ist und im Extremfall Gefahren für Patienten möglich sind, stellt sich die Frage: Sollten die bezahlten Beobachtungen ganz verschwinden?
Tatsächlich sind vereinzelt solche Forderungen zu hören. So hat der heutige Gesundheitsminister und langjährige SPD-Gesundheitspolitiker Karl Lauterbach, selbst Mediziner, am 27. Juni 2020 auf Twitter geschrieben: "Sogenannte Anwendungsbeobachtungen von Medikamenten sollten verboten werden. Sie sind eine legale Art der Korruption."
So weit gehen die wenigsten Experten. Dass sich aber etwas ändern sollte, darin sind sich alle einig – außer den Vertretern der Pharmaindustrie.
Zum Beispiel könnte die Rolle der Ethikkommissionen gestärkt werden. Derzeit ist es nicht verpflichtend, eine Beobachtung vorher dort einzureichen. Größere Firmen tun das aber. Allerdings sind die Kommissionen unzureichend ausgestattet: Ihre Mitglieder sehen die Anträge in ihrer Freizeit durch. Ihr Votum ist nicht bindend.
Eine weitere Möglichkeit betrifft die Prüfung durch die Stellen, denen die Beobachtungen vorab gemeldet werden müssen: Bundesbehörden und Krankenkassen. Sie veröffentlichen zwar diese Meldungen und später auch den Abschlussbericht. Sie bewerten aber beides nicht: Weder was das Honorar angeht noch den wissenschaftlichen Wert.
Forderung nach mehr Transparenz
Ein grober Fehler, findet der Strafrechtler Ralf Kölbel. Dann würde die Meldung auch einen Zweck verfolgen: "Tatsächlich ist es so, dass die Meldungen auf Halde gelegt werden. Das heißt, es gibt dann die entsprechende Datenbank. Die wird in diesen Einrichtungen vorgehalten, ohne dass dann irgendjemand etwas damit anfängt. Es besteht auch keine gesetzliche Verpflichtung."
Der Gesetzgeber habe eine sehr merkwürdige Konstruktion bei der Statuierung der Meldepflichten gewählt und sie damit begründet, dass so eine gewisse Transparenz entstehe. Die würde genügen, um korruptiven Beziehungen entgegenzuwirken."
Tatsächlich ist es aber eine Schein-Transparenz – und das, obwohl nicht immer nur kleine Scheine den Besitzer wechseln. Die Arzneimittelkommission der Deutschen Ärzteschaft, ein Organ der Bundesärztekammer, hat Medizinern deshalb vor Kurzem davon abgeraten, sich an Anwendungsbeobachtungen zu beteiligen.
Patienten können ablehnen
Ralf Kölbel ist das zu wenig: Der Gesetzgeber müsse sich entscheiden – und damit zuerst einmal wir, als Gesellschaft und als Patienten. Wollen wir also, dass Ärztinnen und Ärzte von Pharmafirmen Geld dafür bekommen, dass sie unsere Behandlungen beobachten? Oder sollten solche Daten nur im Rahmen von kontrollierten Studien gesammelt werden, die von staatlicher Seite wirklich beaufsichtigt werden?
"Wenn ich sage, ich will diese Interessenkonflikte, die Anwendungsbeobachtungen offenbar immanent sind, nicht haben, dann bleibt mir nichts übrig, als Anwendungsbeobachtungen ganz zu untersagen. Ich kann mich natürlich auch auf einen anderen Standpunkt stellen und kann sagen: Vernünftig durchgeführte Anwendungsbeobachtungen erfüllen einen bestimmten Zweck. Für diesen Zweck nehme ich es in Kauf, dass gleichsam in der Nebenwirkung gewisse verschreibungsstimulierende Wirkungen eintreten. Wenn ich mich auf diesen Standpunkt stelle, kann ich es so lassen, wie es ist. Was ich aber jedenfalls machen muss als Gesetzgeber: entweder explizit den einen oder explizit den anderen Weg gehen."
Bisher bleibt uns als Patientinnen und Patienten nichts anderes übrig, als diese Entscheidung selbst zu treffen. Und zwar in dem Moment, in dem der Arzt uns sagt: Sie bekommen doch dieses Medikament – da wüsste die Herstellerfirma gerne, wie es sich bewährt. Man kann dann unterschreiben, dass das in Ordnung geht. Und darauf vertrauen, dass das den Arzt bei der Therapie nicht beeinflusst. Man kann aber auch skeptisch sein und Nein sagen.
Das Feature wurde erstmals am 22.10.2020 gesendet.