Die Hoffnung, wieder laufen zu lernen
07:06 Minuten

Die Hoffnungen von Menschen mit Lähmungen sind groß: Elektrische Stimulationen über Rückenmarks-Implantate sollen dabei helfen, sich allein bewegen zu können. Kann die Technologie tatsächlich dabei helfen, wieder gehen zu lernen?
"Das sind alles Amateure hier. Ich glaube, sie wissen gar nicht, was sie tun…"
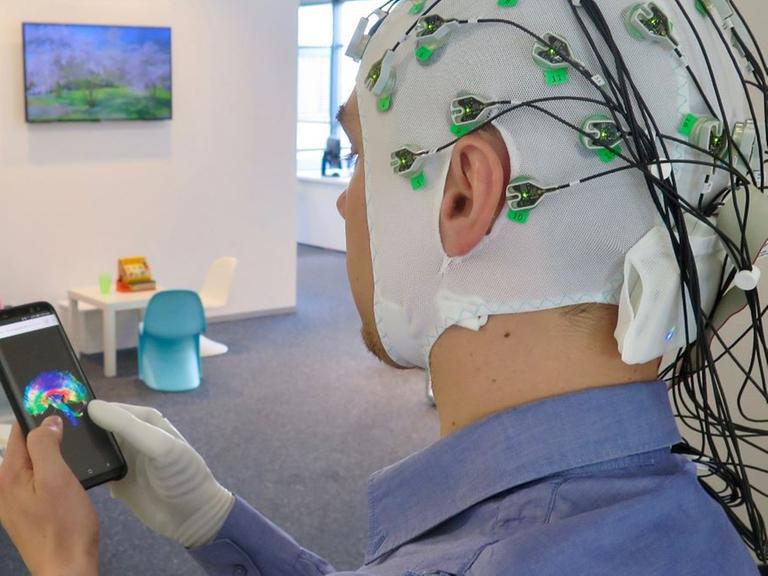
Als David Mzee diese Worte in eine Kamera flüstert, sitzt er in einem Rollstuhl – in einem Labor des Schweizer Federal Institut of Technology in Lausanne. Es ist Ende 2016 – und er ist Teil einer Studie der Neurowissenschaftler Grégoire Courtine und Jocelyn Bloch. Sie wollen Verletzungen des Rückenmarks behandeln. Und zwar so, dass querschnittsgelähmte Menschen ihre Bewegungsfähigkeit wiedererlangen. In einer mehrstündigen Operation wurden David Mzee dafür Elektroden ins Rückenmark implantiert.
Erstes Ergebnis: "Wir haben ihn gebeten, einen kleinen Schritt mit seinem linken Bein zu machen. Und dann einen größeren – ohne die Intensität der Stimulation zu erhöhen. Und man kann sehen, dass die Restfasern, die bisher stillgelegt waren, nicht nur den gelähmten Muskel aktivieren, sondern ihm auch ein gewisses Maß an Kontrolle über die Aktivität des Muskels geben."
2010 verletzte sich David Mzee – damals Student der Sportwissenschaften in Zürich – beim Training. Ein Salto missglückte, seither ist er querschnittsgelähmt. Der Chefarzt der Reha-Klinik vermittelte den Kontakt zu Grégoire Courtine.
Dieser hatte da schon rund zehn Jahre zu Rückenmarksverletzungen an Ratten geforscht – und festgestellt: "Auch wenn die Region im Rückenmark, die normalerweise einen Muskel kontrolliert, intakt ist – dann ist die Ratte trotzdem komplett gelähmt. Und zwar, weil diese Region durch die Verletzung vom Gehirn abgetrennt wurde. Wenn jetzt also das Ratten-Gehirn ein Kommando ans Rückenmark schickt – dann ist das Signal unterbrochen."
Unversehrte Nervenstränge reaktivieren
Bei seinen Untersuchungen des Rückenmarks um die verletzten Stellen herum stellte Grégoire Courtine allerdings fest, dass häufig einige Nervenstränge erhalten bleiben – anatomisch unversehrt, funktional aber stillgelegt. Er versuchte daraufhin, das inaktive Rückenmark einer Ratte über elektrische Stimulation zu reaktivieren.
"Das Tier fing sofort an zu laufen! Und zugleich konnte die Stimulation die Funktionalität der verbliebenen Nervenfasern wieder herstellen. Wir haben unserem Versuchstier ein Stück Schokolade vor die Nase gehalten, ein Sinnesreiz. Das Hirn interagierte daraufhin mit dem Rückenmark, die Ratte begann sogar zu springen. Als wir die Schokolade wegnahmen, war die Ratte frustriert. Die Bewegung stoppte. Wir hatten offenbar wirklich die Kommunikation zwischen Hirn und Rückenmark unter der Verletzung wieder in Gang gesetzt."
"Die haben auf der Höhe im Rückenmark, wo die Beine repräsentiert sind, eine Elektrode eingesetzt, epidural. Ist aus Silikon und hat 16 Einzelkontakte drauf. Und diese kann man dann differenziert ansteuern – und mit dieser Stimulation kann man Reflexbogen auslösen, die dann die Beine muskulär ansteuern."
Damit das gelingt, musste Jocelyn Bloch jede Einzel-Elektrode hochpräzise positionieren, nach einem zuvor erstellten personalisierten Modell. Zum Zeitpunkt der Operation ist dabei noch nicht klar, ob die Erkenntnisse aus der Forschung mit Ratten auf den Menschen übertragbar sind. Innerhalb etwa eines halben Jahres nach der OP aber schafft es David, mehr als 100 Meter mit einem Rollator zu laufen – und anderthalb Stunden auf dem Laufband, eingehängt in Tragegurte.
Nachwachsen von Nervenfasern
Und er überrascht die Forscher mit einer Entdeckung: "Ihr habt mich gefragt, wie lange ich letzte Nacht geschlafen habe. Fünf Stunden. Weil ich aufgewacht bin und die Zehen am linken Fuß überprüft habe.."
David Mzee konnte die Zehen bewegen.
"… und es funktioniert immer noch – nicht mehr so wie gleich nach dem Aufwachen, aber .. ja! Ist das diese Plastizität?"
Bei den Ratten konnte das Team um Grégoire Courtine und Jocelyn Bloch per Magnet-Resonanz-Verfahren Plastizität nachweisen. Das heißt: die Tatsache, dass die verbliebenen Nervenfasern während der Therapie mit Elektrostimulation teilweise nachwuchsen oder sich neu verbunden haben. Beim Menschen, so Edeny Baaklini vom Zentrum für Neuroprothetik am Schweizer Institute of Technology, steht dieser Nachweis noch aus.
"… da wir nach der Implantation keine Magnetresonanz mehr machen dürfen. Wir gehen aber davon aus, dass beim Menschen genau dieses Sprießen auch zustande kommt, da wir bei Patienten gesehen haben, dass sie sich nach fünf Monaten intensivem Training mit der Elektrostimulation – die haben da gewisse motorische Fähigkeiten zurückerlangt und haben Bewegungen sogar ohne Stimulation durchführen können."
Dass David Mzee inzwischen mehrere hundert Meter gehen kann – teilweise freihändig – ist derzeit noch das Ergebnis eines Zusammenspiels von Willen, Algorithmen, die präzise steuern, wann welche Stelle im Rückenmark stimuliert wird – und Sensoren, die Bein- und Fußstellungen messen und an das Implantat zurückmelden.
"Wenn nur die Elektrode allein aktiv ist, zucken die Muskeln ein wenig und mehr nicht. Und wenn ich alleine versuche, kann ich nur ganz wenig Bewegung ausführen. Und wenn die beiden Signale zusammentreffen: mein willkürlicher Input und die Elektrodenstimulation – dann entstehen Schreitbewegungen."
Hartes Training vonnöten
In Zukunft lassen sich die Hirnsignale möglicherweise auch direkt über ein Implantat im Motorcortex auslesen und an eine Rückenmarks-Elektrode weiterleiten. Bei Affen konnten die Forscher so bereits Gehbewegungen initiieren.
"Beim Menschen sind wir leider noch nicht so weit", sagt Edeny Baaklini. "Da arbeiten wir nicht-invasiv mit EEGs, um die Hirnsignale zu lesen und dadurch eine Bewegung auslösen zu können. Und den Übergang vom Gehirn zur unteren Extremität durch die Elektrode wiederherstellen zu können."
Bis dahin bleibt jeder gelungene Schritt vor allem: das Resultat von hartem Training.
"Ich hab das Gefühl, dass hands-free trainieren, also freihändig, wirklich das ist, was am meisten bringt. Und deshalb trainiere ich zuhause freihändig. Und im Moment 2 bis 3 Mal die Woche. Was ein Riesenaufwand ist. Jedes Mal. Das ganze Zeugs anzuziehen, auch mental bereit zu sein, etcetera. Weil, wir wissen nicht, wie oft man trainieren muss, wie genau man trainieren muss – das gilt es alles noch herauszufinden. Wir wissen nicht, ob mehr wirklich besser ist, aber im Moment sieht‘s schon danach aus.
Im Alltag ist es zum Beispiel das Drehen im Bett, das geht. Da wacht man nachts auch etwas weniger auf, weil es einfacher geht. Aber zum Beispiel auch, wenn man zugeparkt wird im Auto, dann kann ich aufstehen, ein bis zwei Schritte nach vorne gehen, einsteigen, zurückfahren und dann den Stuhl reinnehmen. Das sind so kleine Dinge. Ja – was wir wissenschaftlich geschafft haben, ist schon cool und beeindruckt mich selbst immer wieder."